Das deutschsprachige HL7 Magazin
inklusive Interview mit Gustav Vella, Carelane GmbH, Bremen
FHIR hatte in den Anfängen seinen Schwerpunkt in punkto Abdeckung mit Ressourcen sicherlich auf die Patientenversorgung. In jüngster Zeit aber hat auch der Bereich für die Unterstützung Klinischer Studien große Erweiterungen und Verbesserungen erfahren.
Die internationale HL7-Community arbeitet schon seit Jahrzehnten daran, Forschung und Versorgung einander näher zu bringen. Noch allerdings werden in Deutschland die Möglichkeiten der gemeinsamen internationalen Entwicklungen etwaiger FHIR-Ressourcen und Profile zu wenig genutzt bzw. eine breite deutsche Beteiligung auf internationalem Parkett wird nicht gelebt. Zwar gibt es in Deutschland die Medizininformatik-Initiative MII, das Vorhaben Informationstechnische Systeme in Krankenhäusern ISiK und Interoperabilität für IT-Systeme in Pflegeeinrichtungen ISiP oder auch die Kassenärztliche Bundesvereinigung mit den Medizinischen Informationsobjekten MIO, doch braucht es Geduld, bis diese Bemühungen zur nationalen Nutzung von FHIR beim Benutzer ankommen. Der Anspruch, hier internationale Reichweite zu erlangen und in den entsprechenden Gremien mitzuwirken, muss erst noch verinnerlicht werden, damit er über das Engagement der Expertinnen und Experten von HL7 Deutschland hinaus intensiviert wird.
Ein Beispiel dafür sind klinische Studien und die Unterstützung durch HL7 FHIR sowohl bei Planung, als auch die Durchführung. In diesem Beitrag wollen wir ein wenig den Stand der Dinge und die Hintergründe beleuchten und mit einem ausgesprochenen Experten und Macher auf dem Gebiet, Gustav Vella, darüber sprechen.
Das Gesundheitswesen hat den Schwung zur Digitalisierung, der durch die Pandemie ausgelöst wurde, genutzt und hat zum Beispiel im Bereich der Nutzung von Daten aus Versorgung für die Forschung dazugelernt.
Sowohl die normierten Informationen über die klinische Studie selbst (Metadaten), die Unterstützung des Ablaufs der Studien selbst, als auch die interoperable Einbindung der Informationsquellen, zum Beispiel Krankenhausinformationssysteme oder Apps, sind hier essenziell. Jeder Schritt innerhalb einer Studie ist aktuell noch immer eine Hürde. Definition, Recruiting, Consent und Vorbereitungen sind für das Studienmanagement eine Herausforderung, die folgende Durchführung mit der Datenerhebung, Auswertung und Nachbetrachtung sind inhaltlich und logistisch anspruchsvoll.
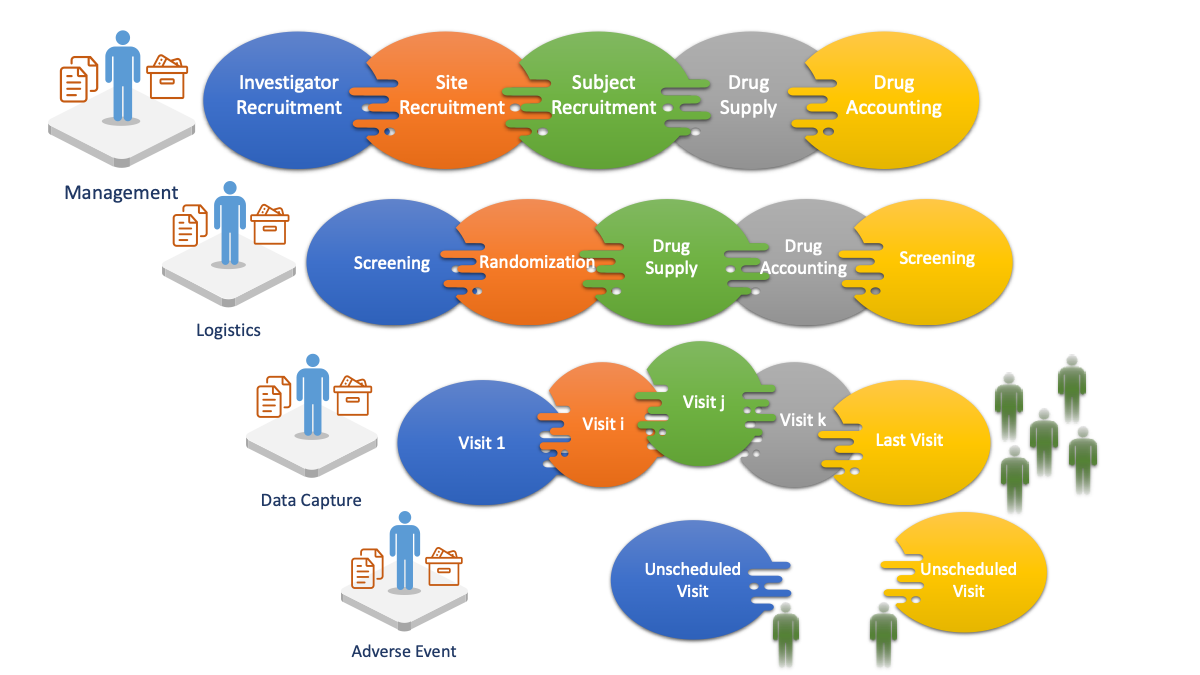
Abbildung 1: Der „Geschäftsprozess“ klinische Studie in den Aspekten Management, Logistik Datenerhebung usw. (Quelle Dr. Kai U. Heitmann, CEO, HL7 Deutschland, Experte HL7 Europe: HL7 Standards für Studien, im Workshop zum Gesundheitsdaten-Nutzungsgesetz GDNG, Berlin, 5. April 2024)
Die HL7 FHIR Ressourcen ResearchStudy und ResearchSubject sollen hier zunächst für die studienbeschreibenden Daten klinischer Studien eine gute Unterstützung liefern. Auch im Sinne optimierter und standarisierter Erfüllung der Informations- und Transparenzpflicht bei klinischen Studien kann HL7 FHIR gut eingesetzt werden.
| Studienbeschreibende Daten |
|---|
|
In der Zusammenschau gibt es ein ganzes Portfolio an Lösungen, ein FHIR Information Model für Klinische Studien, wie schon von Leroux et. al. 2019 beschrieben.
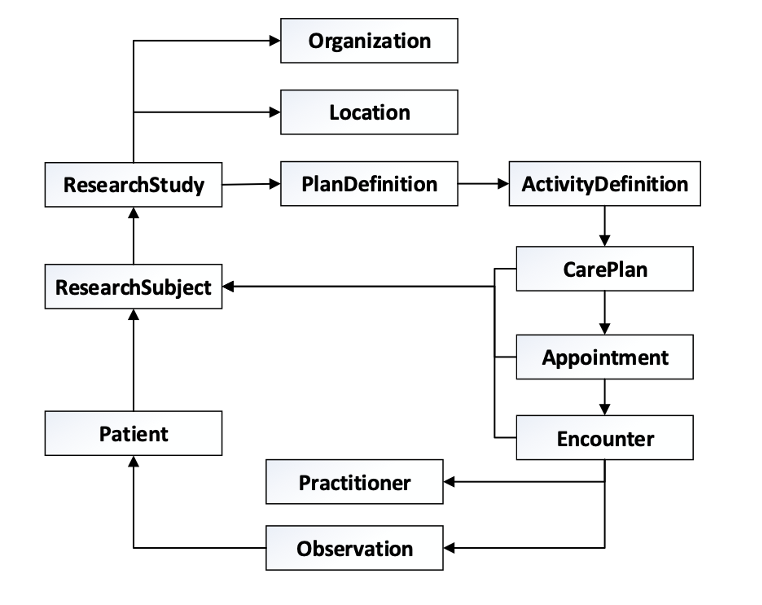
Abbildung 2: FHIR Information Model für Klinische Studien (aus: Hugo Leroux, Christine K Denney, Smita Hastak, Hugh Glover: A framework for representing clinical research in FHIR A framework for representing clinical research in FHIR, December 2019, Conference: Semantic Web Applications and Tools for Healthcare and Life Sciences, Edinburgh, Scotland)
FHIR-Ressourcen und Profile ermöglichen die standardisierte Beschreibung einer klinischen Studie und bringen in der praktischen Anwendung klinische Systeme dazu, standardisiert definierte Studien zu unterstützen und den Patientenfluss transparent darzustellen. Dafür engagiert sich die internationale HL7 Community mit seinen Entwicklerinnen und Entwicklern aus der ganzen Welt beteiligen. Aus Deutschland ist die Unterstützung noch gering – dabei gibt es hierzulande besonders viel zu gewinnen. Gustav Vella, HL7-Experte und Gründer der Carelane GmbH, Bremen, und Kontributor in der HL7 Biomedical Research and Regulations Working Group (BRR) wirkt hier seit längerer Zeit in den internationalen HL7-Gremien mit. Kai Heitmann, CEO HL7 Deutschland, sprach mit ihm.
Kai Heitmann: An welchen Profilen arbeitet Ihr derzeit in den FHIR-Arbeitsgruppen „Klinische Studien“?
Gustav Vella: Neben vielen kleineren Projekten haben wir große, gute Schritte für die Unterstützung klinischer Studien gemacht. Da ist einmal die Ressource ResearchStudy und die ResearchSubject, die sich beide mit dem Design und der Durchführung klinischer Studie beschäftigen.
| Zweck der Research Study Ressource |
|---|
|
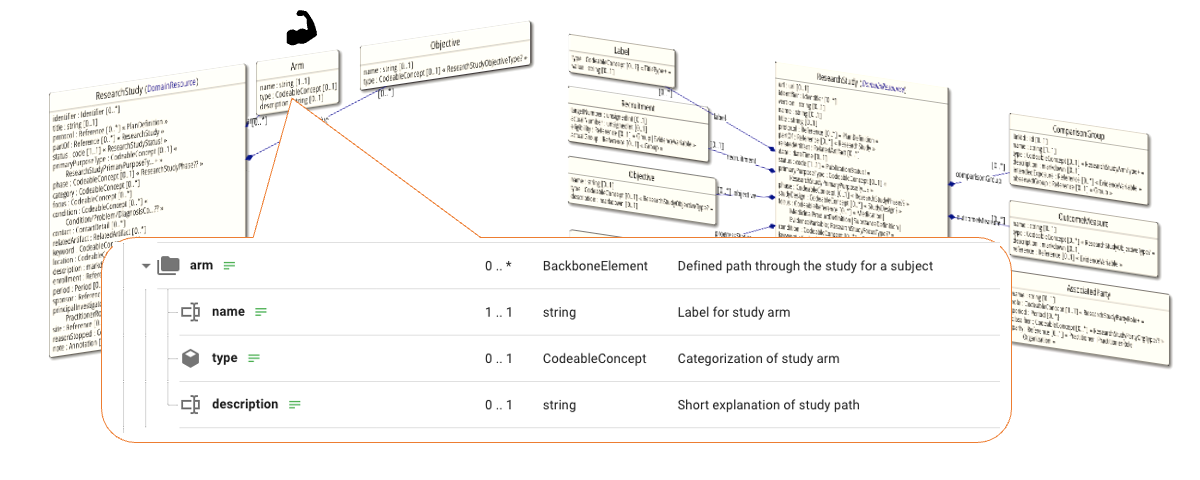
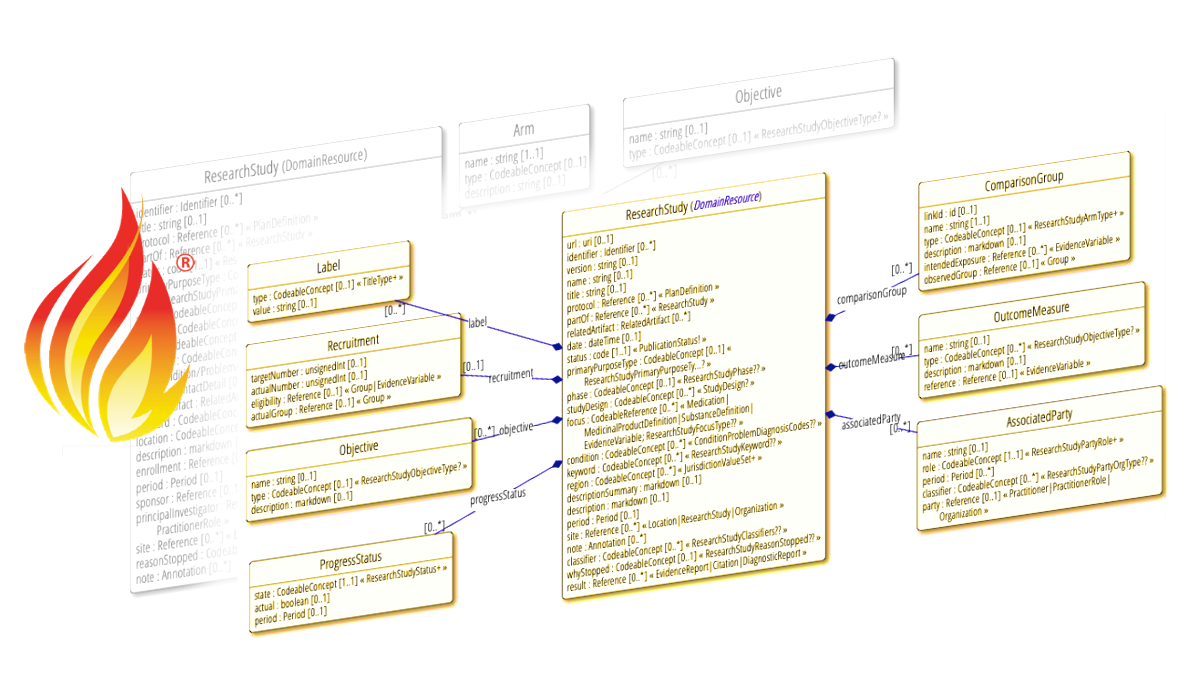
Abbildung 3: Andeutungen des FHIR Models für Klinische Studien, links Release 4 und rechts Release 5 – alles ist reifer geworden.
| Research Study in FHIR R5 (und R6) |
|---|
|
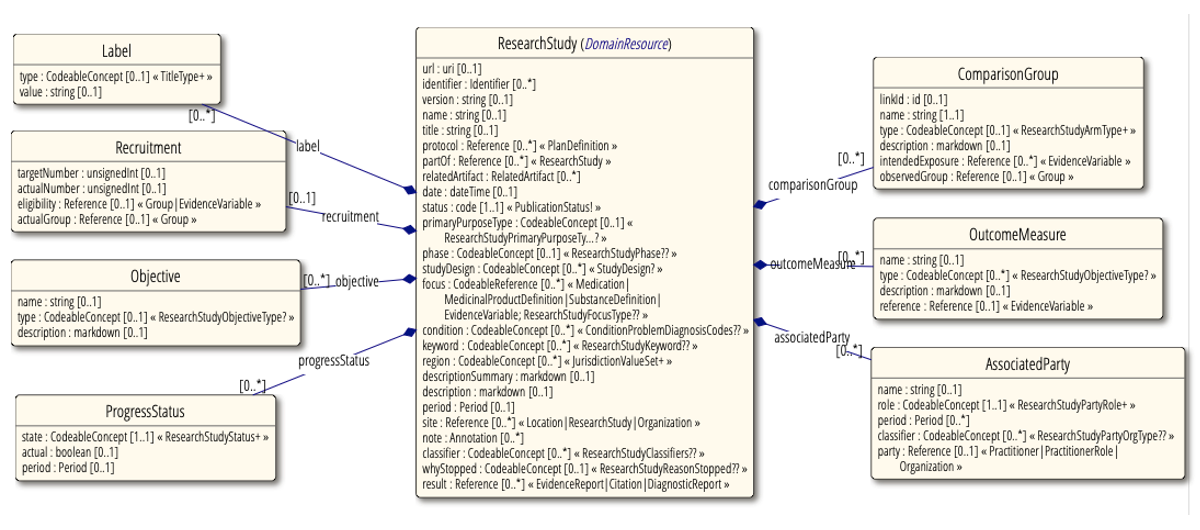
Abbildung 4: das FHIR Models für Klinische Studien aus dem Release 6 – noch vorläufig aber weise.
ResearchStudy beschäftigt sich mit dem Protokoll und dem eigentlichen Ablauf einer Studie, ResearchSubject reflektiert den Studienteilnehmenden und begleitet den Patientenfluss während der Studie – vom Pre-Screening bis zum Anschluss. Dabei gibt es gerade in Deutschland große Schwierigkeiten, wie ich Dir nicht verraten muss.
Kai Heitmann: Worin bestehen diese Schwierigkeiten aus Deiner Sicht?
Gustav Vella: Die Abbildung einer Studie in deutschen Krankenhausinformationssystemen (KIS) ist eine Seltenheit. Die meisten Systemhersteller haben Studien nicht verstanden oder wollen sie nicht verstehen. Es braucht aber für die Praktikabilität eine Schnittstelle, die kommunizieren muss und Informationen, die den Patienten betreffen, weitergeben kann.
Auch für die Klinik ist es wichtig, den aktuellen Stand zu kennen: ist der Patient in der Studie oder nicht, hat die Patientin zugestimmt etc. Wir haben es jetzt so weit überarbeitet, dass der gesamte Ablauf auf einen Blick eingesehen werden kann. Auch der regulatorische Bereich ist transparent dargestellt.
Kai Heitmann: Zu welchem Release von FHIR rätst du aktuell, um sich die Möglichkeiten offen zu halten?
Gustav Vella: Best Practice wäre aus meiner Sicht, etwas höher zu skalieren. Wer heute eine Studie designed / modelliert, sollte auf jeden Fall auf R6 auch jetzt schon benutzen. Dafür werden ja nur „Definitional Resources“ genutzt, das heißt die Definitionen, die das Projekt modellieren, können alles abbilden, was notwendig ist. Aber du hast sonst keine Abhängigkeit zu irgendwelchen Downstream-Systemen.
Allerdings muss man schauen, worum es im Einzelnen geht. Die Kriterien in Abfragen sollten auch zu niedrigeren FHIR-Versionen transferiert werden können. In USA bzw. in den EPIC-Häusern operieren die meisten auf einer R4 Ressource und FHIR Path Expressions.
Wenn die Ressourcen aber mit den Ressourcen im KIS interoperabel sein sollen, dann muss eine Downstream-Portierung umgesetzt werden. In Deutschland hat man ja etwas „überprofiliert“ – mit KBV, ISiK, ISiP und MII haben wir oft jeweils vier Profile für dasselbe. Wenn man jetzt die Daten aus dem Primärsystem extrahiert, muss die Group Ressource an die ursprünglichen Ressourcen angepasst werden.
Kai Heitmann: Aber die Vorteile überwiegen klar, oder?
Gustav Vella: Tatsächlich ist es auch jetzt schon eine große Erleichterung. Ein Protokoll, welches die gleiche Sprache spricht wie die Downstream-System macht es ungemein einfacher, die Daten aus den Downstream-Systemen rauszuholen. Und das ist seit Anfang diesen Jahres 2024 möglich.
Kai Heitmann: In Deutschland ist es schwer, Leute zu motivieren, sich an den internationalen Entwicklungen zu beteiligen – in anderen Ländern ist es selbstverständlicher, freiwillig oder gar reguliert gemeinsam an etwas Internationalem zu arbeiten. Welche erfolgversprechenden Möglichkeiten der Beteiligung gibt es denn aktuell? Wer beschäftigt sich mit diesen FHIR-Ressourcen?
Gustav Vella: Ich bin ein Fan des Vulcan-Accelerators, der im Übrigen ebenfalls klar auf FHIR setzt. Regierungsbehörden und Technologie-Unternehmen haben sich zusammengetan mit dem Ziel, klinische Forschung voranzubringen, indem wissenschaftliche Forschungsgemeinschaften mit Unternehmen zusammengebracht werden. Auch hier spielt FHIR eine große Rolle beispielsweise für die Definition der Studienprotokolle. Und darum geht es, wir müssen Systeme bauen, die wiederum Protokolle in der Sprache der Primärsysteme bauen können. Deswegen haben sie HL7 und andere wie CDISC und ICH involviert. Du siehst, es ist auf jeden Fall lohnend in FHIR zu investieren und mitzumachen.
Die Exklusions-Inklusions-Kriterien für eine klinische Studie in FHIR abzubilden ist einfach traumhaft.
Gustav Vella

| Beschleuniger VULCAN! HL7 FHIR for Clinical Research |
|---|
Der Vulcan FHIR Accelerator verleiht der Nutzung von FHIR für die klinische Forschung neue Impulse
Ziele: Entwicklung von Vulcan-Implementierungsleitfäden, Vulcan-Projekte zu Real World Data und Schedule of Activities |
Kai Heitmann: Und an welchen Stellen kann man mitarbeiten?
Gustav Vella: Hier gibt es konkret eine Arbeitsgruppe, die dreimal wöchentlich (Di/Mi/Do) zu unterschiedlichen Uhrzeiten zusammenkommt und miteinander denkt.
Kai Heitmann: Die HL7 Biomedical Research and Regulations Working Group (BRR) sprichst du an. Sie hat vieles gebracht, aber was fehlt noch?
Gustav Vella: Aus meiner Sicht sind die Plandefinitionen für die Abbildung der Studien-Visiten im Protokoll relativ ausgereift. Aber was fehlt, sind die Geschäftslogik und die Beziehungen in den Einzelelementen in den Protokollen. Welche Auswirkungen hat die Auswahl – wie sehen die Beziehungen untereinander aus? Oder auch, wie eine Study Definition Terminologie definiert werden kann, wie CDISC-Vokabular in FHIR abzubilden ist, dafür gibt es ebenfalls gerade Arbeitsgruppen.
Im Grunde geht es dennoch vor allem darum, das Rad nicht neu zu erfinden. Gerade in der Medizininformatik-Initiative wird das aus meiner Sicht an zu vielen Stellen doch versucht. Dort wurden, wo also noch nicht so viel da war, sehr viele eigene Extensions definiert, einen Mechanismus den FHIR ja anbietet. Aber das will man ja gerade eben nicht, weil das ja keine Sache ist, die, sagen wir mal, den Standard an der Stelle unterstreicht, sondern man möchte die Anforderung in die Weiterentwicklung einbringen. Da gibt es viele Ansätze, die bereits durch die Community breiter entwickelt wurden.
Es ist auf jeden Fall lohnend für klinische Forschung, in FHIR zu investieren!
Gustav Vella
Kai Heitmann: Ja, da gebe ich Dir recht. Die vielen Extensions sind schwierig, weil sie die Standards unterminieren.
Gustav Vella: Ja genau. Mein Rat: Erst einmal auf FHIR R4 setzen. Das wird überall gemacht und die brauchbaren Systeme können das meistens. FHIR R6 sollte natürlich dennoch das Ziel sein und man kann schon jetzt viel von R6 für heute lernen.
Kai Heitmann: Vielen Dank, Gustav, dass du uns ein paar Einsichten gegeben hast in die neuesten Entwicklungen zu FHIR-Ressourcen für klinische Studien. Bleibt vielleicht unser gemeinsamer Aufruf, dass sich auch aus Deutschland mehr Expertinnen und Experten berufen fühlen, hier bei den internationalen Entwicklungen mitzumachen. Danke.
…haben Gulden et al 2021 schon Ergebnisse veröffentlicht, wie die Studieninformationen in (damals noch nicht zureichende) FHIR Ressourcen zu mappen und standardiert auszuwerten sind. Dabei wurde der FHIR Server nicht nur zur Kommunikation, sondern auch für Datenhaltung (Persistenz) und Auswertung (Search) verwendet. Christian Gulden, Romina Blasini, Azadeh Nassirian, Alexandra Stein, Fatma Betül Altun, Melanie Kirchner, Hans-Ulrich Prokosch, Martin Boeker: Prototypical Clinical Trial Registry Based on Fast Healthcare Interoperability Resources (FHIR): Design and Implementation Study. in JMIR Med Inform 201 Jan; 9(1)
… hat Gustav Vella schon auf dem Treffen des Deutschen Interoperabilitätsforums in Köln im Juni 2023 über die notwendigen Anpassungen und bisherigen Arbeiten einen Vortrag gehalten, der hier nochmals zu sehen ist.
Bildnachweis: HL7 Deutschland